对于吸入制剂测试,控制温度、相对湿度 (RH) 和静电至关重要。了解原因…
当吸入制剂测试数据 (尤其是多级撞击器测量) 的可变性达到不可接受的程度时,优化流量控制或许是解决之道。或者,如果问题与操作员相关,就用自动化技术应对。但测试环境呢?这会是问题所在吗?
您是否考虑过实验室在一天之中乃至一年四季的温度和相对湿变化,以及这些因素对测量的影响?您的静电消除策略的有效性和稳定性如何?
在吸入制剂测试中,局部环境的温度、相对湿度和静电效应均是潜在关键可变性来源。而且它们很容易被忽视。本博客主要介绍环境控制、环境控制的重要性以及如何实现环境控制。
测试环境如何影响吸入制剂测试数据?
这个基本问题有两个不同的解决方法:(1) 通过影响剂量递送 (2) 通过影响多级撞击器性能。
经口吸入制剂 (OIP) 的剂量递送是一个动态过程。致动触发后向患者或测试仪器释放一定剂量的雾化制剂,但剂量的特性并非固定不变。影响这些特性的因素会左右各种形式的OIP测试。
此外,多重可变性来源会影响多级冲击器性能乃至气动粒度分布 (APSD) 测量。
测试环境中的可变性会通过与这两个问题相关的机制影响吸入制剂测试,总结如下。
温度
温度通过支配汽化速率 (尤其是推进剂的汽化速率) 直接影响剂量分散度。由于粘度、表面张力等特性与温度相关,它还会进一步影响雾化表现。
至于测试设备,撞击器内部的液滴蒸发风险也与温度相关,进而影响APSD测量结果。根据药典规定,雾化吸入剂测试过程中需要将新一代撞击器 (NGI) 冷却至5oC,这恰恰突显了这个问题的重要性i、ii;同样,软雾吸入制剂测试的现行最佳实践也建议进行冲撞击器冷却iii。此外,温度变化也会影响测量准确性和流量控制,而后者是保证撞击器分离性能稳定性的必要条件。
相对湿度
相对湿度会左右剂量递送过程中的颗粒/液滴形成过程,从而影响递送剂量的特性。对于液体和粉末配方都是如此,粉末解聚尤其容易受到湿度的影响。
静电
剂量分散的能量性质会导致摩擦生电,即通过接触和分离产生静电荷。因此,在测试过程中更容易诱发静电效应。这是一个需要严谨研究的复杂领域,但众所周知的是,静电效应会影响撞击器重的剂量分散和沉积行为。因此,静电产生和消散的可变性可能会带来问题。
尽管上述任一因素中均会单独影响测试数据,但它们之间的相互作用会使可变性影响更加复杂化。例如,温度和相对湿度共同影响雾化过程,从而决定了分散液体配方的特性。而相对湿度对静电有显著影响。由于水具有很强的导电性,静电效应在较高相对湿度,也就是40 – 60%的条件下并不明显,这样即可确保将大量静电荷导向大地。
缓解环境可变性的策略
NGI冷却
根据药典规定,雾化吸入剂测试过程中应冷却NGI,这就需要执行冷藏。一种方法是在实验室冷藏箱中冷却撞击器 (通常需要约90分钟),然后在明显升温前完成测试。另一种方法是使用专门解决此类的设备,例如NGI降温柜。它可在0 – 10oC范围内提供节能温控能力。
常规测试环境控制
为了更全面地控制吸入制剂测试环境,人们自然会想到对实验室进行空调 (A/C – 温度)或全气候控制 (温度 + 相对湿度)。遗憾的是,此类系统的前期和运行成本令不少人望而却步。在一些会加重系统工作负荷的地区,或者如果能源安全、可靠性和成本存在问题,这个问题会尤为突出。
此外,即使已经安装空调或气候控制系统,也有必要检查它们保持工作站内环境恒定性的实际效果。使用中的设备释放的热量、气流、窗户和通风口位置都会对局部环境产生潜在影响。
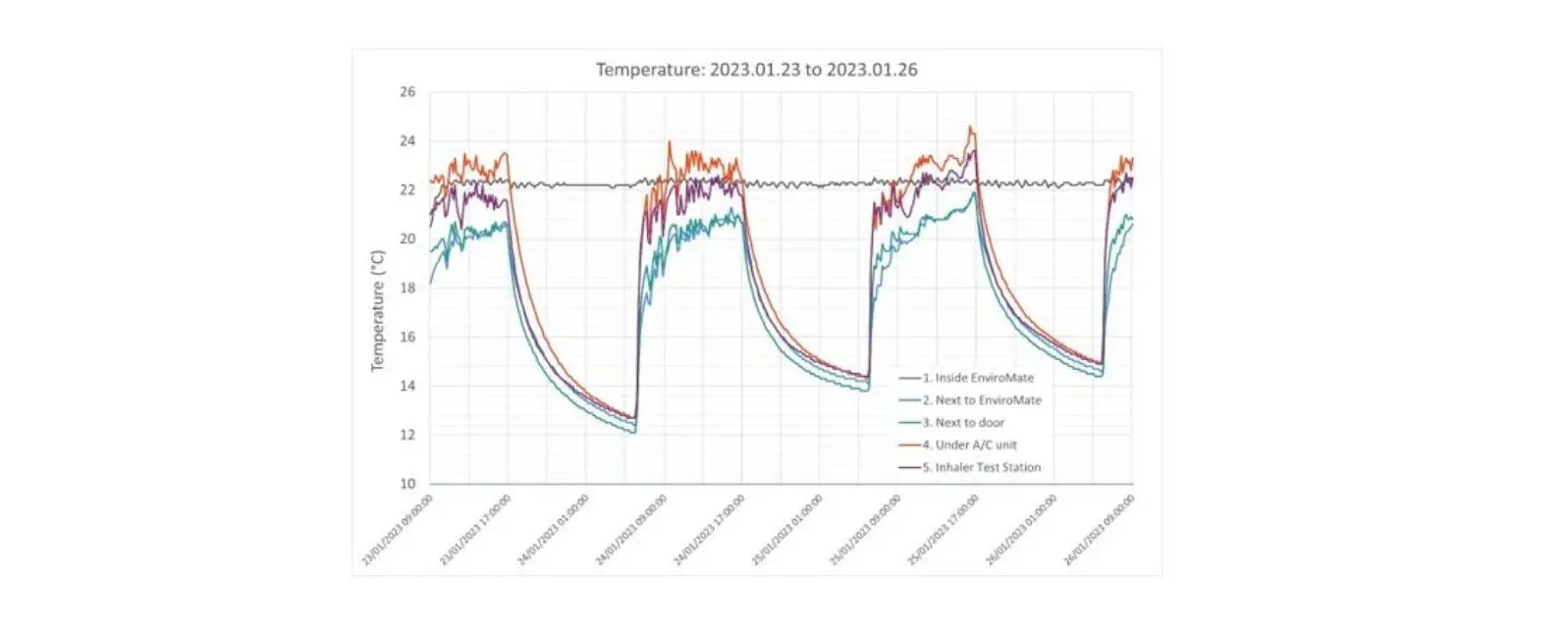
实验室环境控制系统的替代方案是使用单体气候控制试验箱。这些设备非常有效,提供灵活性和统一控制能力,而且前期和运行成本相对较低。例如,EnviroMate™是我们专为吸入制剂测试设计的台式设备,全程提供精确的温度 (+/-2oC) 和相对湿度 (+/-5%) 控制。同时内置防静电系统,最大限度减少静电效应。
关注静电
稳健的温度和相对湿度控制是最大限度减少静电效应的重要第一步,但其他措施也能提供帮助/起到关键作用。实用策略包括:
- 设备和操作员均采取接地措施
- 限制手套的使用和佩戴类型
- 选择正确的实验室防护装备,防静电鞋就是一个很好的例子
- 部署静电消除器、除静电枪和离子棒
手持式静电计可用于检查所采取的静电缓解措施的有效性。
如需进一步了解环境控制的影响和益处,请阅读我们的白皮书。您将从中了解到测试环境的多变性,以及更重要的是,这对测试数据意味着什么。通过改善数据完整性和减少错误的超标/超常测试结果,环境控制优化可以让研发乃至质量控制部门享受切实红利。为了确保最高级别的数据完整性,这绝对值得考虑。
i USP <1601> Products for nebulization – Characterization tests
ii Ph. Eur. 2.9.44 Preparations for nebulisation: characterisation
iii J. Mitchell et al ‘Good Practices for the Laboratory Performance Testing of Aqueous Oral Inhaled Products (OIPs): an Assessment from the International Pharmaceutical Aerosol Consortium on Regulation and Science. AAPS PharmSciTech (2023) 24:73








